DIE SÄURE DES BODENS
Boden, als Umgebung für Pflanzenwachstum und -entwicklung, kann sauer sein, neutral oder alkalisch. Erklären, Wovon hängt eine solche Reaktion ab?, Sie müssen wissen, was in der Chemie als Dissoziation von Wasser bekannt ist. Es geht darum, dass einige Wassermoleküle in Wasserstoffatome zerfallen, eine positive elektrische Ladung tragen (daher sind sie mit dem Symbol H + gekennzeichnet und werden als Wasserstoffionen bezeichnet), und auf den sog. Hydroxid-Ionen, elektrisch negativ geladen und mit dem Symbol OH gekennzeichnet . Das Vorherrschen positiver H * -Wasserstoffionen ist die Ursache für den Säuregehalt der Umgebung, während das Vorherrschen negativer OH-Hydroxidionen seine Basizität bestimmt, auch Umweltalkalinität genannt.
Gründliche Recherche hat gezeigt, dass sehr wenige Wassermoleküle dissoziieren, z.B. Bei einer Temperatur von 25 °C enthält ein Liter Wasser nur ein Zehnmillionstel Gramm H und genau so viele Gramm-Ionen OH . Zur Vereinfachung wird eine verkürzte Schreibweise mit der Potenz mit negativem Exponenten verwendet, und so 0,0000001 = 10 hoch -7. Es ist in einem Liter sauberem Wasser 10 hoch -7 "saure" Ionen” ich 10 hoch -7 "alkalische Ionen."”. Bei der Bestimmung der Reaktion der Umgebung wurde die Konzentration an Wasserstoffionen als Maß genommen. Aus dem lateinischen Namen des Exponenten der Konzentration von Wasserstoffionen [Wasserstoffkraft) diese Konzentration wird mit dem Symbol pH bezeichnet. Denn in einem reinen Liter (destilliert) Wasser, Also in einer neutralen Umgebung, ist 10 hoch -7 Wasserstoffionen von H +, der pH-Wert ist 7. Wenn Sie diesem Wasser eine Prise Limette hinzufügen würden, dann würde die Zahl der OH-Ionen zunehmen , gleichzeitig verringerte es die Zahl der H + -Ionen, und die Reaktion wird alkalisch. Also denk daran, dass der neutrale pH-Wert gleich ist 7. Dieser Indikator zeigt eine neutrale Reaktion an. Reaktion unten 7 bedeutet Versauerung der Umwelt, Oben 7 bedeutet alkalische Reaktion.
 In der landwirtschaftlichen Praxis wird der pH-Wert des Bodens durch Kalken reguliert. Im Allgemeinen sollten mineralische Böden einen pH-Wert haben 6,0-6,5; leichte Böden sollten keinen höheren pH-Wert haben als 5,5-6,0. Mittlere und schwere Böden sollten so gekalkt werden, damit der pH-Wert ab 6,5 tun 7,5. Der Grad der Bodenversauerung (mit etwas Annäherung) lässt sich am einfachsten wie folgt bestimmen: Nehmen Sie die Erde auf eine Untertasse und gießen Sie ein paar Tropfen Essig darüber. Wenn es einen Teardown gegeben hat, meint, dass der Boden kalkreich ist.
In der landwirtschaftlichen Praxis wird der pH-Wert des Bodens durch Kalken reguliert. Im Allgemeinen sollten mineralische Böden einen pH-Wert haben 6,0-6,5; leichte Böden sollten keinen höheren pH-Wert haben als 5,5-6,0. Mittlere und schwere Böden sollten so gekalkt werden, damit der pH-Wert ab 6,5 tun 7,5. Der Grad der Bodenversauerung (mit etwas Annäherung) lässt sich am einfachsten wie folgt bestimmen: Nehmen Sie die Erde auf eine Untertasse und gießen Sie ein paar Tropfen Essig darüber. Wenn es einen Teardown gegeben hat, meint, dass der Boden kalkreich ist.
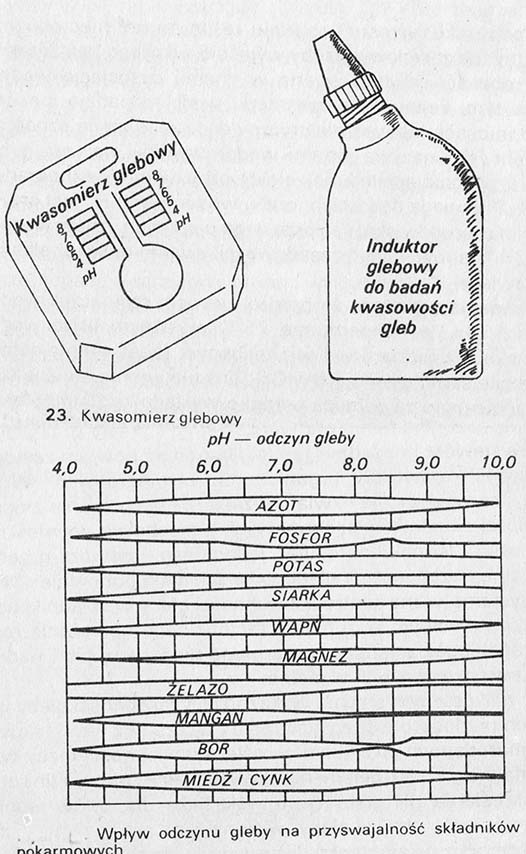
Eine genauere Bestimmung des Kalkungsbedarfs kann mit einem Bodensäuremessgerät erfolgen. Das Hellig-Säuremessgerät ist weit verbreitet. Es ist ein sehr einfaches Instrument, die aus einem Teller und einer Flasche mit einem Indikator besteht. Auf der Tafel befindet sich eine Farbskala, Nut und Längsnut. Eine Prise Erde wird in die Rille gegossen und mit dem Indikator gegossen. Abhängig vom pH-Wert des Bodens hat die erhaltene Lösung die entsprechende Farbe. Die pH-Einstellung besteht darin, diese Farbe der Lösung mit der Skala auf der Platte oder auf einem separaten farbigen Papiereinleger zu vergleichen. Genauere Daten können erhalten werden, indem die Probe an eine chemisch-landwirtschaftliche Station geschickt wird.
Der Einfluss der Bodenreaktion auf Pflanzen ist vielfältig; es kann direkt und indirekt sein. Bestimmte Pflanzengruppen benötigen einen bestimmten Boden-pH-Wert. In den meisten Fällen ist die indirekte Wirkung der Reaktion auf die Pflanze wichtiger, weil es hauptsächlich die Löslichkeit verschiedener Mineralien im Boden beeinflusst. Auf sauren Böden, z.B.. eine übermäßige Menge solcher Inhaltsstoffe entsteht, wie: Knie, Eisen, mangan, und deshalb werden sie für Pflanzen schädlich. Die aufgeführten Inhaltsstoffe wirken sich negativ auf beide Pflanzenwurzeln aus, sowie die Verdaulichkeit der Nährstoffe.
Der Einfluss der Reaktion auf die Verdaulichkeit der Nährstoffe ist in der Abbildung dargestellt. Daran sieht man, diese Reaktion hat den größten Einfluss auf die Bioverfügbarkeit: Phosphor, Eisen, Manganu und Boru. Je niedriger der pH-Wert ist, die Verfügbarkeit von Phosphor ist geringer, während die anderen drei Nährstoffe im alkalischen Zustand schwer zugänglich sind. Mit zunehmender Bodensäure steigt die Aktivität von Eisen, Ton und Mangan. Unter diesen Bedingungen werden lösliche Phosphate stark an diese Komponenten gebunden, wodurch sehr komplexe und nicht verdauliche Beziehungen entstehen. Wenn der pH-Wert des Bodens deutlich überschritten wird 7, Die Pflanzenernährung wird sonst gestört. Umfassend gebildet werden, unlösliche Calciumphosphate, die nicht nur die Bioverfügbarkeit von Bodenphosphor reduzieren, aber auch Phosphordünger. Die Verdaulichkeit von Nährstoffen hängt also stark vom pH-Wert des Bodens ab. Eine gute Versorgung der Pflanzen mit Nährstoffen steigert nicht nur die Erträge von Gemüse und Obst, aber es wirkt sich auch auf ihre Qualität aus, und vor allem der Gehalt an mineralischen Verbindungen in ihnen, wird von Ernährungswissenschaftlern als die beste Quelle für Mineralsalze für den menschlichen Körper angesehen.
Auch der pH-Wert des Bodens beeinflusst die Entstehung von Pflanzenkrankheiten. Ich nehme np. Säurereaktion fördert die Entstehung von Kohlsyphilis, Falscher Mehltau der Zwiebel, a reduziert die Schorfbildung bei Kartoffeln.
